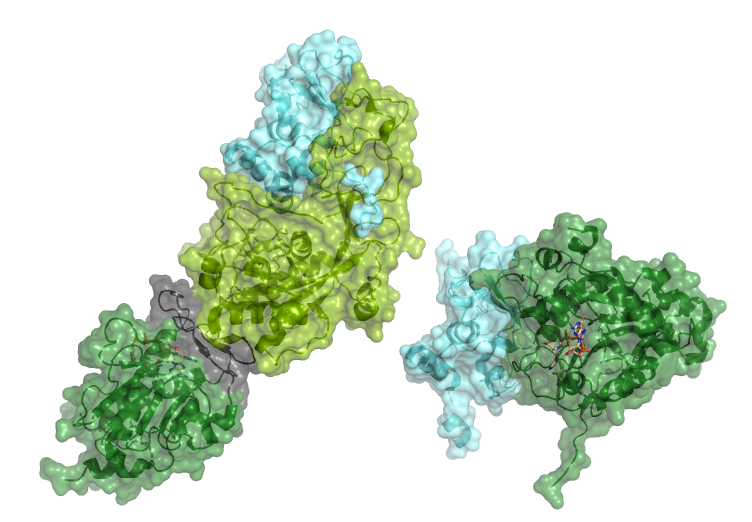
SARS-CoV-2 besitzt zwei Methyltransferasen, Nsp14 (auch bekannt als Exonuklease) und Nsp16. Beide erzeugen „Methylkappen“ an RNA, die generell die RNA vor Abbau schützen und auch für die mRNA-Prozessierung und angeborene Immunität wichtig sind. Das Protein Nsp10 (hellblau) aktiviert beide Methyltransferasen.
Nsp16 (dunkelgrün, rechts) hat Methyltransferaseaktivität für den 2’-Sauerstoff der viralen RNA.
Nsp14 (Exonuklease) besitzt zwei Funktionen in zwei Domänen, mit einer Domäne, die sie flexibel verbindet (grau). Die N-terminale domäne (hellgrün, links) hat eine Exoribonuklease-Funktion, die neu produzierte RNA in 3‘-5’Richtung überprüft und so Mutagenese verhindert (siehe auch: RNA Polymerase). Diese Funktion gestattet es SARS-CoV-2, ein so großes Genom zu haben, mit 29.8 Kilobasen Länge.
Andere RNA-Viren wie Hepatitis C (9.6 Kilobasen) oder Lassavirus (zwei RNA-Ketten mit 3.4 und 7 Kilobasen Länge) haben kein solches Enzym und haben folglich wesentlich kleinere Genome.
Die C-terminale Domäne (dunkelgrün, im linken Bild) hat Methyltransferase-Aktivität für das 5’-Ende der viralen mRNA.
Es wurde zwar bisher keine Nsp14-Struktur aus SARS-CoV-2 gelöst, aber die bekannte SARS-CoV-Struktur hat 95% Sequenzidentität.